Las palabras de la ciencia (II): ion, anión, catión y otras palabrejas eléctricas.
Por Lorenzo Hernández • 10 Dic, 2015 • Sección: Hablar de CienciaLa historia empieza con Faraday (1791- 1867) que, combinando sus aficiones por la química y la electricidad, hizo algunos descubrimientos críticos sobre los efectos de pasar corrientes eléctricas a través de soluciones químicas. Otros científicos antes que él realizaron electrolisis, como el inglés Humphrey Davy, que realizó la primera electrolisis, o los ingleses Carlisle y Nicholson, que en 1800 realizaron la primera descomposición del agua por efecto de la corriente eléctrica, pero su entendimiento de lo que ocurría era tan distinto de los sostenido previamente que, en 1834, publicó un artículo en el Philosophical Transactions de la Royal Society que introducía seis nuevos términos en el reino de la ciencia.

Michael Faraday, 1861
En lugar de llamar «polo» al objeto que los científicos colgaban de una solución, Faraday introdujo la palabra electrodo. Al electrodo en que se depositaban los gases como el oxígeno y el cloro, que se cargaban negativamente al pasar una corriente a través de una solución, lo llamó ánodo, y llamó cátodo al electrodo donde se depositaban los elementos químicos cargados positivamente. Lo que se liberaba de cualquiera de los electrodos fue llamado electrolito. Éstos se dividían en aniones, que se recogían en el ánodo, y cationes, que se extraían del cátodo.
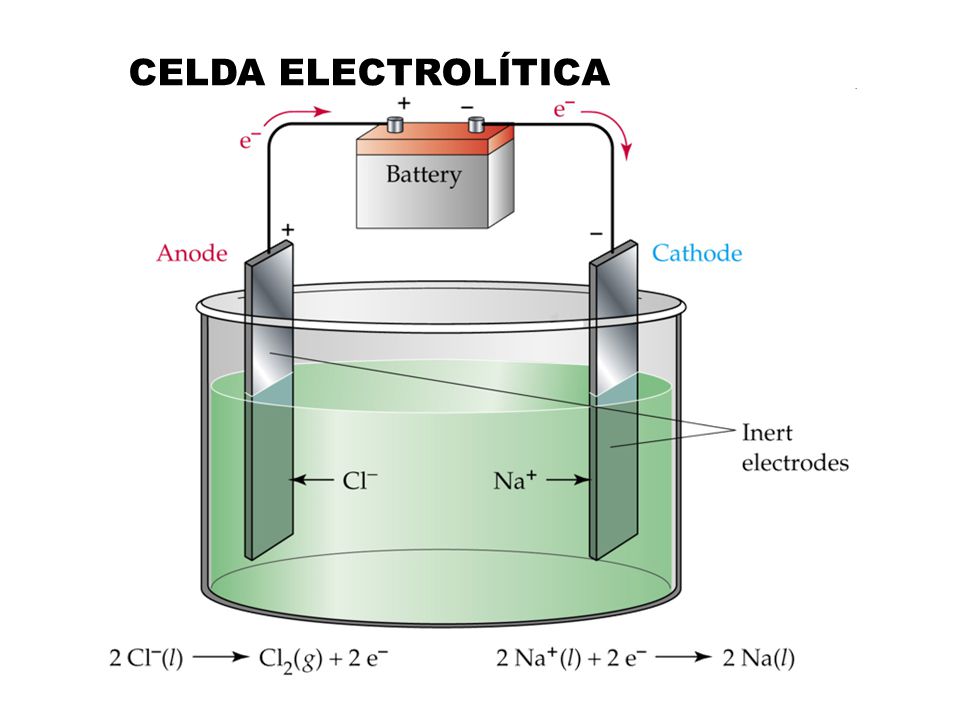
Imagen 2: esquema de una celda electrolítica.
¿Pero tiene alguna relación la nomenclatura que propuso Faraday con lo que representa? Pues sí, ya que los iones, tanto los aniones como los cationes, se desplazan a través de la solución hacia el ánodo y hacia el cátodo.
Ion es una palabra griega que significa «ir, el que camina». El prefijo cata- significa «hacia abajo» y el prefijo an- «hacia arriba». Reflejan el hecho de que los iones de cargas opuestas se mueven en sentidos contrarios en presencia de un campo eléctrico. De modo parecido cátodo proviene de cata (hacia abajo) + hodos (camino). Aunque literalmente signifca camino hacia abajo, Faraday la usó para referirse a un electrodo con carga negativa, del cual fluye la corriente hacia el de carga positiva al que llamó, como ya sabemos, ánodo y significa camino hacia arriba.
Respecto a la palabra electrolito proviene de élécktron (electricidad) y lytos (soluble). Por tanto, un electrolito es una sustancia que se disuelve cuando se aplica electridad.
Ya sabemos el significado de las palabras pero es interesante el resto de la historia para conocer la naturaleza de esos iones. Para ello siguamos comentando algunas pinceladas de lo que ocurrió.
Así pues, Faraday establecido las leyes de la electrólisis, y a juzgar por ellas parecía que la electricidad, igual que la materia, podía existir en forma de pequeñas partículas. Como he dicho, Faraday había hablado de iones, que podían considerarse como partículas que transportaban electricidad a través de una disolución. Sin embargo, durante el medio siglo siguiente, ni él ni nadie más, se aventuró a trabajar seriamente sobre la naturaleza de aquellos iones. Lo cual no significó, sin embargo, que no se hiciese ningún trabajo valioso. En 1853, el físico alemán Johann Wilhelm Hittorf (1824-1914) señaló que algunos iones viajaban más rápidamente que otros. Esta observación condujo al concepto de número de transporte, la velocidad a la que los distintos iones transportaban la corriente eléctrica. Pero el cálculo de esta velocidad no resolvía la cuestión de la naturaleza de los iones.
Como indiqué en el post anterior la teoría atómica no fue totalmente aceptada hasta principios del siglo XX, por lo que en el último cuarto del siglo XIX había científicos que no creían en ella. Es el caso del químico ruso-germano Friedrich Wilhelm Ostwald (1853-1932), el más importante de esa época en el campo de la química física. Gracias a él más que a ninguna otra persona, la química física llegó a ser reconocida como una disciplina con derecho propio. Hacia 1887 había escrito el primer libro de texto sobre el tema, y fundó la primera revista dedicada exclusivamente a la materia. Pero Ostwald fue un seguidor de los principios del físico y filósofo austriaco Ernst Mach (1838-1916), quien creía que los científicos debían tratar sólo de materias que fuesen directamente mensurables, y no debían crear «modelos» basados en pruebas indirectas. Por esta razón, Ostwald rehusó aceptar la realidad de los átomos, ya que no existían pruebas directas de su existencia. Fue el último científico importante que se resistió a la teoría atómica (aunque no negaba su utilidad, por supuesto)*.
Otro gran científico de la época fue, al cual sólo aventajaba Ostwald en el campo de la química física, fue Van’t Hoff. Trabajó en especial sobre problemas de soluciones. Hacia 1886 logró demostrar que las moléculas de sustancias disueltas, moviéndose al azar a través de la masa de líquido, se comportan en cierto sentido de acuerdo con las reglas que rigen el comportamiento de los gases.
El nuevo estudio de la química física relacionaba las reacciones químicas no sólo con el calor, sino más bien con la energía en general. La electricidad, por ejemplo, podía producirse por reacciones químicas y originar, a su vez, reacciones químicas.
Walther Hermann Nernst, un alemán (1864-1941), aplicó los principios de la termodinámica a las reacciones químicas que ocurrían en una batería. En 1889 demostró que las características de la corriente producida pueden usarse para calcular el cambio de energía libre en las reacciones químicas que producen corriente.
Junto a Ostwald y Van’t Hoff estaba otro maestro de la naciente química física, el químico sueco Svante August Arrhenius (1859-1927). Siendo estudiante, Arrhenius dirigió su atención a los electrolitos: esto es, a aquellas disoluciones capaces de transportar una corriente eléctrica.

Imagen 3: Svante Arrhenius (1909)
Arrhenius encontró la manera de abordar el asunto gracias al trabajo del químico francés François Marie Raoult (1830-1901). Como Van’t Hoff, Raoult estudió las disoluciones. Sus estudios culminaron en 1887, con el establecimiento de lo que ahora se llama ley de Raoult: la presión de vapor parcial del solvente en equilibrio con una disolución es directamente proporcional a la fracción molar del solvente. Esta regla permitió estimar el número relativo de partículas (ya fueran átomos, moléculas, o los misteriosos iones) de la sustancia disuelta (el soluto) y del líquido en el que estaba disuelta (el disolvente).
En el curso de esta investigación, Raoult había medido los puntos de congelación de las disoluciones. Tales puntos de congelación eran siempre más bajos que el punto de congelación del disolvente puro. Raoult logró mostrar que el punto de congelación descendía en proporción al número de partículas de soluto presentes en la disolución.
Pero aquí surgía un problema. Era razonable suponer que cuando una sustancia se disuelve en agua, pongamos por caso, dicha sustancia se rompe en moléculas separadas. Efectivamente, en el caso de no-electrolitos como el azúcar, el descenso del punto de congelación cumplía dicha suposición. Sin embargo, cuando se disolvía un electrolito como la sal común (NaCl), el descenso del punto de congelación era el doble de lo que cabía esperar. El número de partículas presentes era el doble del número de moléculas de sal. Si se disolvía cloruro bárico (BaCl2), el número de partículas presentes era tres veces el número de moléculas.
La molécula de cloruro sódico está formada por dos átomos, y la de cloruro bárico por tres. Así pues, Arrhenius pensó que al disolver determinadas moléculas en un disolvente como el agua, se descomponían en átomos separados. Además, puesto que tales moléculas, una vez rotas, conducían una corriente eléctrica (pero no así las moléculas como el azúcar, que no se descomponen), Arrhenius sugirió que las moléculas no se rompían (o «disociaban») en átomos ordinarios, sino en átomos que llevaban una carga eléctrica.
Arrhenius propuso que los iones de Faraday eran simplemente átomos (o grupos de átomos) que llevan una carga eléctrica positiva o negativa. Los iones, o eran los «átomos de electricidad», o portaban a los «átomos de electricidad». (La última alternativa demostró posteriormente ser la correcta.) Arrhenius utilizó su teoría de la disociación iónica para dar cuenta de numerosos hechos de electroquímica.
*Más tarde hizo su aparición en escena el tema del movimiento browniano. Este fenómeno, que implica el movimiento rápido e irregular de pequeñas partículas suspendidas en agua, fue observado por primera vez en 1827 por un botánico escocés, Robert Brown (1773-1858). El físico germano-suizo Albert Einstein (1879-1955) demostró en 1905 que este movimiento puede atribuirse al bombardeo de las partículas por moléculas de agua. Como en un momento dado puede haber más moléculas golpeando desde una dirección que desde otra, las partículas serán impulsadas ahora hacia acá, ahora hacia allá. Einstein elaboró una ecuación para calcular el tamaño real de las moléculas de agua después de medir ciertas propiedades de las partículas en movimiento. Un físico francés, Jean Baptiste Perrin (1870-1942), hizo las medidas necesarias en 1908, y obtuvo la primera estimación segura del diámetro de las moléculas y, por tanto, de los átomos. Dado que el movimiento browniano era una observación razonablemente directa de los efectos de las moléculas individuales, hasta el mismo Ostwald tuvo que abandonar su oposición a la teoría atómica.
Referencias:
- Asimov, Isaac. (1975). Breve historia de la química. Alianza.
- Atkins, Peter William (2015) ¿Qué es la química? Alianza Editorial.
- Moore, Pete (2003). Las grandes ideas que formaron nuestro mundo. Lisma Ediciones, S.L.
- Diccionario etimológico: http://etimologias.dechile.net/
- Imagen 1: https://es.wikipedia.org/wiki/Michael_Faraday
- Imagen 2: http://images.slideplayer.es/14/4268708/slides/slide_23.jpg
- Imagen 3: https://upload.wikimedia.org/wikipedia/commons/9/92/Svante_Arrhenius_01.jpg
Esta entrada participa en la LIII edición del Carnaval de Química, alojada en el blog quimidicesnews de @quimidicesnews.

[…] Las palabras de la ciencia (II): ion, anión, catión y otras palabrejas eléctricas. de Lorenzo Hernández desde el blog cienciaonline.com Share this:LinkedInGoogleTwitterFacebookCorreo electrónicoMe gusta:Me gusta Cargando… […]